Ключевые факты о лейкемии
Что такое лейкемия?
Какие выделяют типы лейкемии?
Каковы факторы риска, повышающие опасность развития лейкоза?
Какие симптомы лейкоза встречаются?
На основании чего ставится диагноз лейкемии?
Какое лечение предстоит при лейкемии?
Нужно ли другое мнение перед началом лечения?
Нужна ли поддерживающая терапия при лейкозе?
Какое значение имеют питание и физическая активность при лейкемии?
Потребуется ли наблюдение по окончании курса терапии?
Почему важно организовать поддержку для больных лейкемией?
Что собой представляют клинические испытания при лейкозе?
Ключевые факты о лейкемии
- Лейкемия является раком клеток крови.
- Хотя точная причина лейкемии не известна, факторы риска ее были идентифицированы давно.
- Общие симптомы хронического или острого лейкоза могут включать боль в костях и суставах, увеличение лимфатических узлов, как правило, не болезненных, лихорадку или ночную потливость, чувство слабости или усталости, кровотечения и беспричинные синяки, частые инфекции, отек или дискомфорт в животе и потерю веса или аппетита.
- Лейкозы дифференцируются по нескольким признакам. По тому, как быстро болезнь развивается, выделяют острый и хронический процесс. В зависимости от типа клеток крови, пораженных опухолью, бывает лимфоцитарный (лимфоциты) и миелоцитарный (миелоциты) процесс. Четыре основных типа лейкемии включают: острый лимфобластный лейкоз (ОЛЛ), хронический лимфоцитарный лейкоз (ХЛЛ), острый миелолейкоз (AML) и хронический миелолейкоз (ХМЛ).
- Люди с лейкемией имеют значительно повышенный риск развития инфекций, анемии, кровотечения. Другие симптомы и признаки включают образование небольших малозаметных синячков, потерю веса, ночную потливость и необъяснимую лихорадку.
- Диагноз лейкемии подтверждается на основании симптомов и диагностики, заключающейся в изучении образцов крови и костного мозга под микроскопом.
- Выбор лечения лейкемии зависит от типа лейкоза, определенных особенностей лейкозных клеток, стадии заболевания, предшествующей истории лечения, а также от возраста и состояния здоровья пациента.
- Большинство пациентов с лейкемией лечатся с помощью химиотерапии. Некоторые пациенты также могут подвергаться лучевой терапии и/или трансплантации костного мозга.
- На сегодняшний день нет никакого известного способа предотвратить лейкемию.
- Прогноз при лейкемии зависит от нескольких факторов, включая возраст пациента, тип лейкемии и степень распространенности опухолевого процесса.
Что такое лейкемия?
Лейкемией является рак, который начинается в тканях, образующих кровь. Чтобы понять, как появляется заболевание, уделим немного времени тому, как образуются нормальные клетки крови.
Нормальные клетки крови
Большинство клеток крови развивается из первичных клеток, называемых стволовыми клетками костного мозга. Костный мозг является мягким веществом, расположенным в канале, имеющемся в большинстве трубчатых костей.
Стволовые клетки мозга при созревании превращаются в различные виды клеток крови. Каждый вид выполняет особую функцию:
- белые кровяные клетки. Лимфоциты способствуют активной борьбе с инфекцией. В организме каждого из нас их насчитывается несколько видов.
- красные кровяные клетки. Эритроциты помогают переносить кислород к тканям и органам по всему телу.
- тромбоциты. Это клетки, участвующие в формировании кровяных сгустков - тромбов, служащих для прекращения кровотечения.
Белые кровяные клетки, эритроциты и тромбоциты происходят от стволовых клеток, и организм остро нуждается в них. Когда клетки стареют или получают какие-либо повреждения, они умирают, а новые клетки спешат занять их место.
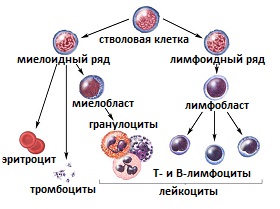
Рис.1 Процесс дифференцировки (взросления) клеток крови
У человека с лейкемией костный мозг вырабатывает неправильные белые клетки крови. Эти аномальные клетки и являются клетками лейкемии. В отличие от нормальных клеток, поврежденные клетки лейкоза не умирают в отведенные им сроки. Поэтому их может выработаться настолько много, что они смогут вытеснить обычные белые кровяные клетки, эритроциты и тромбоциты. Подобный процесс не дает крови выполнять возложенную на нее защитную и газотранспортную функцию, от чего страдает весь организм.
Какие выделяют типы лейкемии?
Типы лейкемии могут быть сгруппированы на основе того, насколько быстро болезнь развивается, и пациенту становится все хуже. Заболевание может характеризоваться:
- хроническим (медленно ухудшающимся);
- острым (быстро ухудшающимся) течением.
Хронический лейкоз. Это заболевание имеет свои характерные черты. В начале заболевания лейкозные клетки могут выполнять некоторые функции нормальных белых кровяных клеток. Из-за чего никаких достоверных данных о наличии заболевания, на первый взгляд, не имеется. Однако это не так, поскольку результаты анализов уже на столь ранней стадии показывают ненормальный состав крови. Поэтому хронический лейкоз часто обнаруживают во время обычной проверки, т.е. еще до появления каких-либо симптомов.
Постепенно состояние больного хроническим лейкозом ухудшается. По мере увеличения числа лейкозных клеток в крови появляются такие симптомы, как увеличение лимфатических узлов или частые инфекции. На ранней стадии симптомов не так много, но по мере того, как функционирование лейкозных клеток ухудшается, а число нормальных белых клеток сокращается, состояние становится все хуже.
Острый лейкоз. Заболевание характеризуется тем, что видоизмененные лейкозные клетки с самого начала не могут выполнять функции нормальных белых кровяных клеток. Число лейкозных клеток возрастает быстро, а вместе с этим быстро ухудшается состояние пациента.
Помимо остроты течения тип заболевания также зависит от того, какой тип клеток вовлечен в патологический процесс. Лейкоз может начаться в лимфоидных или миелоидных клетках. Лейкемия, проистекающая из лимфоидных клеток, называется лимфоидной. Это лимфоцитарный или лимфобластный лейкоз. Лейкемия, начинающаяся с изменения миелоидных клеток, называется миелоидной. Это миелолейкоз или миелобластный лейкоз.
Современная классификация лейкоза
В медицине различается четыре основных типа лейкоза:
- Хронический лимфолейкоз (ХЛЛ). Заболевание проистекает из лимфоидных клеток и обычно характеризуется крайне медленным развитием. На его долю приходится более 15 000 новых случаев лейкемии, фиксируемых каждый год. Чаще всего заболевают люди, чей возраст старше 55. Подобный тип лейкоза почти никогда не встречается у детей.
- Хронический миелоидный лейкоз (ХМЛ). Заболевание начинается с миелоидных клеток и, как правило, на первых порах развивается достаточно медленно и неагрессивно. На его долю приходится почти 6 000 новых случаев лейкемии, фиксируемых каждый год. Это заболевание тоже встречается в основном у взрослых.
- Острый лимфобластный лейкоз (ОЛЛ). Заболевание происходит из лимфоидных клеток и характеризуется крайне быстрым развитием. На его долю приходится более 6 000 новых случаев лейкемии ежегодно. ОЛЛ является наиболее распространенной формой лейкемии у детей раннего возраста, однако также может встречаться и у взрослых.
- Острый миелоидный лейкоз (ОМЛ). Заболевание начинается с миелоидных клеток и характеризуется быстрым ростом. На его долю приходится более 18 000 новых случаев лейкемии, фиксируемых каждый год. Встречается болезнь, как у взрослых, так и у детей.
Есть еще волосатоклеточный лейкоз, который является редким типом хронического лейкоза.
Каковы факторы риска, повышающие опасность развития лейкоза?
К большому сожалению, официальная медицина не знает, что является отправной точкой в изменении деятельности костного мозга, продуцирующего кровяные тельца. Поэтому сказать, почему тот или иной человек заболел, не получится. Тем не менее, исследования показывают, что определенные факторы риска все же есть. И они увеличивают вероятность того, что человек заболеет лейкозом.
Факторы риска могут быть различными для различных типов лейкозов. Но в основном это:
- Радиация. Люди, подвергнувшиеся воздействию очень высокой дозы радиации, имеют больше шансов, чем другие, заболеть острым миелоидным лейкозом, хроническим миелоидным лейкозом или острым лимфобластным лейкозом.
- Атомные взрывы. Очень высокие уровни радиации были зафиксированы в ходе взрывов атомных бомб (таких, как в Японии во время Второй Мировой Войны). Люди, особенно дети, которые выживают после атомных взрывов, подвергаются повышенному риску лейкемии.
- Лучевая терапия. Еще один источник воздействия высоких уровней радиации, к которому прибегают для лечения рака и ряда других заболеваний. Лучевая терапия может повысить риск лейкемии.
- Диагностические рентгеновские лучи. Стоматологические рентгеновские лучи и другие диагностические рентгеновские лучи (например, КТ) подвергают людей гораздо более низким уровням радиации. О том, связан ли подобный уровень облучения с лейкемией, достоверных фактов нет. Исследователи продолжают изучать данный аспект, среди прочих рассматривая вопрос о том, могут ли частые рентгенографии увеличить риск лейкемии. Они также изучают, может ли КТ, сделанное в детстве, послужить отправной точкой развития лейкемии.
- Курение. Курение сигарет увеличивает риск развития острого миелоидного лейкоза.
- Бензол. Воздействие бензола на рабочем месте может привести к острой миелоидной лейкемии. Это также может вызвать хронический миелоидный лейкоз или острый лимфобластный лейкоз. Бензол широко используется в химической промышленности. Он также содержится в сигаретном дыме и бензине.
- Химиотерапия. У онкологических больных с определенными типами рака после проведенного курса химиотерапии позже может развиться острый миелоидный лейкоз или острый лимфобластный лейкоз. Среди наиболее известных на сегодняшний день провоцирующих веществ медики называют алкилирующие агенты или ингибиторы топоизомеразы. Из-за них иногда развивается острый лейкоз.
- Синдром Дауна и некоторые другие наследственные заболевания. Подобные диагнозы свидетельствуют о наличии определенного риска развития острой лейкемии.
- МДС (Миелодиспластический синдром) и некоторые другие заболевания крови. Люди с определенными заболеваниями крови подвергаются повышенному риску развития острого миелоидного лейкоза
- Вирус Т-клеточного лейкоза человека (HTLV-I). Люди с HTLV-I подвергаются повышенному риску редкого типа лейкемии, называемого «Т-клеточный лейкоз взрослых». Но хотя вирус HTLV-I и может привести к этой редкой болезни, заболевание не является заразным для окружающих.
- Наследственность. Если среди родственников в пределах одной семьи часто фиксируется лейкемия, то, скорее всего, речь идет о хроническом лимфолейкозе. Тем не менее, болезнь редко наследуется через поколение. Поэтому среди больных в одной семье нет родственников с родством первого поколения (отец, мать, ребенок или брат, сестра).
Наличие одного или нескольких факторов риска не означает, что человек обязательно заболеет. Большинство людей, которые имеют факторы риска, никогда не болеют лейкемией.
Какие симптомы лейкоза встречаются?
Как и все клетки крови, лейкозные клетки перемещаются по организму. Симптомы лейкемии зависят от количества лейкозных клеток, и где эти клетки собираются в организме. У людей с хронической лейкемией симптомов может не быть. Однако врач может найти заболевание во время обычного анализа крови.
Люди с острым лейкозом обычно идут к врачу, потому что они чувствуют себя больными. Если поражен мозг, они могут жаловаться на головные боли, рвоту, спутанность сознания, потерю мышечного контроля или судороги. Лейкемия может также повлиять на другие части тела, такие как желудочно-кишечный тракт, почки, легкие, сердце или яички.
Общие симптомы хронического или острого лейкоза могут включать:
- увеличение лимфатических узлов, которые обычно безболезненны (особенно в диагностическом плане важны размеры лимфатических узлов в области шеи или подмышек);
- лихорадка или проливные ночные поты;
- частые инфекции;
- чувство слабости или постоянная усталость;
- кровотечения и кровоподтеки (кровотечение из десен, пурпурные звездочки на коже или крошечные красные пятна под кожей);
- отек или дискомфорт в животе (от раздутой селезенки или печени);
- потеря веса или аппетита по неизвестной причине;
- боль в костях и суставах.
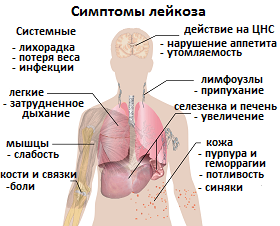
Рис.2 Симптомы лейкоза и системы организма, поражаемые при лейкемии
Чаще всего эти симптомы не связаны с раком. Инфекции или другие проблемы со здоровьем тоже могут являться причиной подобных проявлений. Однако только врач может утверждать это. Но это не значит, что можно оставаться безучастными. Любой человек с этими симптомами должен записаться на прием к врачу, чтобы проблему можно было диагностировать и начать лечить как можно раньше.
На основании чего ставится диагноз лейкемии?
Врачи иногда могут найти лейкемию после обычного анализа крови. Если у человека есть симптомы, указывающие на лейкоз, его лечащий врач будет пытаться выяснить, что вызывает проблемы. Доктору может понадобиться собрать анамнез, включающий вопросы о том, не было ли случаев лейкоза в семье.
При этом также проводится несколько простых тестов:
- Осмотр. Врач проверяет увеличение лимфатических узлов, селезенки и печени.
- Анализы крови. Лаборатория делает полную расшифровку состава крови, чтобы проверить количество белых кровяных клеток, эритроцитов и тромбоцитов. Лейкемия вызывает очень высокий уровень белых кровяных клеток. Это может также привести к снижению уровня тромбоцитов и гемоглобина, который находится внутри красных кровяных клеток.
- Биопсия. Доктор удаляет ткань для исследования на наличие раковых клеток. Биопсия является единственным надежным способом узнать, есть ли клетки лейкемии в костном мозге. Образец берется под местной анестезией, что помогает устранить боль. В ходе биопсии на анализ изымается частичка костного мозга от тазовой или другой большой кости. Патологоанатом использует микроскоп, чтобы проверить ткань на клетки, характерные для лейкемии.
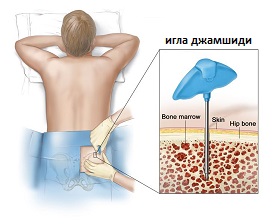
Рис.3 Биопсия костного мозга седалищной кости
Стоит отметить, что есть два способа получить костный мозг. Некоторым пациентам проводят обе процедуры для уточнения диагноза. Речь идет о взятии образцов одного костного мозга или мозга вместе с частью кости.
В некоторых случаях также востребованы и другие тесты. С помощью дополнительного обследования можно определить тип лейкемии и поставить окончательный диагноз. Речь идет о таких обследованиях, как:
- Цитогенетика. В условиях лаборатории специалисты изучают хромосомы клеток, полученных из образцов крови, костного мозга или лимфатических узлов. Если аномальные хромосомы обнаружены, тест может показать, какой тип лейкемии у пациента. Например, люди с ХМЛ обладают ненормальными хромосомами под названием «Филадельфийская хромосома».
- Люмбальная пункция. В ходе исследования врач может взять на анализ часть спинномозговой жидкости (жидкость, которая заполняет пространство вокруг спинного мозга в спинномозговом канале позвоночника). Врач использует длинную тонкую иглу для удаления жидкости из нижней части позвоночника. Процедура занимает около 30 минут и проводится под местной анестезией. В дальнейшем пациент должен лежать в течение нескольких часов, чтобы избежать появления головной боли. Лаборатория проверяет жидкость на наличие лейкозных клеток или других проблем.
- Рентген грудной клетки. В ходе исследования можно увидеть увеличение лимфатических узлов или другие признаки болезни.
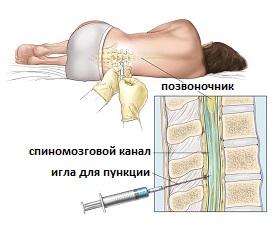
Рис.4 Люмбальная пункция при лейкозе
Какое лечение предстоит при лейкемии?
У людей с лейкемией есть много вариантов лечения. Наиболее распространенными вариантами являются:
динамическое наблюдение;
- химиотерапия;
- целевая терапия;
- биологическая терапия;
- лучевая терапия;
- трансплантация стволовых клеток.
Если селезенка пациента увеличена, врач может предложить операцию, чтобы удалить ее. Иногда также используется сочетание этих процедур. В любом случае, выбор метода не случаен. Лечение зависит в основном от следующих факторов:
- типа лейкоза (острый или хронический, миелоцитарный или лимфоцитарный);
- возраста пациента;
- были ли обнаружены клетки лейкемии в спинномозговой жидкости.
Терапия также может зависеть от некоторых особенностей лейкозных клеток. Врачи, помимо вышесказанного, оценивают симптоматику и общее состояние здоровья больного.
Люди с острым лейкозом должны начинать терапию немедленно. Цель лечения состоит в уничтожении признаков лейкемии в организме до полного исчезновения симптомов. Это называется «ремиссия».
После того, как заболевание переходит в стадию ремиссии, терапия может быть продолжена, чтобы предотвратить рецидив. Этот тип терапии называется консолидационная или поддерживающая терапия. Стоит отметить, что многих людей с острым лейкозом можно вылечить.
В случае с хроническим лейкозом без симптомов, вполне возможно, врач примет решение в пользу выжидательной тактики, на время отложив лечение. При этом пациенту предстоит тщательная регулярная диагностика, которая покажет изменения состояния. Также лечение может быть начато, если у пациента появятся какие-либо симптомы. В медицине подобная тактика получила название «бдительное ожидание».
При лечении хронического лейкоза необходимо тщательно контролировать заболевание и его симптомы. Целью терапии данного заболевания является перевод болезни в стадию устойчивой ремиссии. К сожалению, без пересадки костного мозга при хроническом лейкозе излечение не возможно. Поэтому очень важно добиться полного контроля над болезнью, чтобы сократить вероятность обострения.
Перед началом лечения, в большинстве случаев – химиотерапии, доктор должен сообщить пациенту особенности, ожидаемые результаты и возможные побочные эффекты процесса. Пациент со своей стороны может подсказать врачу ключевые моменты, чтобы разработать план лечения, который не только поможет решить медицинские проблемы, но и позволит больному вести привычную для него активность.
Иногда врач может предложить пациенту принять участие в клиническом исследовании, предполагающем научное изучение новых методов лечения. В этом случае, конечно же, есть и высокая доля риска. Однако если терапия будет успешной, то это сможет продлить жизнь и сделать ее более комфортной.
Лечащий врач также может направить пациента к другому специалисту по собственной инициативе или по просьбе больного. Специалисты, которые лечат лейкемию, это:
- гематологи;
- онкологи;
- радиологи-онкологи;
- детские онкологи;
- детские гематологи.
Помимо лечащего врача в лечебной терапии принимают немалое участие медсестры и врачи-диетологи.
Каждый раз, когда пациент нуждается в стационарном лечении, он должен попасть в медицинский центр, в котором есть специалисты, имеющие опыт в лечении лейкемии. Если это не возможно, то лечащий доктор должен обсудить план лечения со специалистом в таком центре.
Перед началом лечения пациент должен попросить врача объяснить возможные побочные эффекты терапии, а также то, какие изменения в организме она может спровоцировать. Лечение рака часто повреждает здоровые клетки и ткани, так что побочные эффекты могут быть со стороны всех систем организма.
В большинстве случаев переносимость терапии зависит от многих факторов. Поэтому у разных людей побочные симптомы и осложнения могут различаться. Более того, у одного и того же пациента реакция на разные сеансы терапии может быть различной. Важно, чтобы пациент был готов к подобному развитию событий и не потерял веру в себя и собственные силы.
Выжидательная тактика или динамическое наблюдение при лейкозе
У людей с хроническим лимфолейкозом, которые не имеют симптомов, целесообразно отложить лечение рака. Благодаря задержке лечения пациенты могут избежать побочных эффектов терапии, по крайней мере, пока они не имеют симптомов.
Если пациент и его врач пришли к консенсусу, что бдительное ожидание является хорошей идеей, больной лейкозом должен будет посещать больницу для прохождения регулярного осмотра (например, каждые 3 месяца). В случае возникновения симптоматики пациент начнет лечение.
Хотя осторожное ожидание и задерживает побочные эффекты лечения рака, этот выбор имеет свои риски. Это может уменьшить возможность контролировать лейкоз в случае появления симптоматики.
Пациент может решить, когда начитать терапию. И если ему будет некомфортно жить, зная о том, что организм подвержен воздействию клеток лейкемии, можно решиться лечить болезнь сразу. В любом случае, нужно прислушиваться к советам лечащего врача.
Химиотерапия при лейкозе
Многие люди с лейкемией лечатся с помощью химиотерапии. Химиотерапия использует сильнодействующие средства, чтобы разрушить лейкозные клетки. В зависимости от типа лейкоза пациенты могут получать одно лекарство или комбинацию двух или более лекарственных средств.
Введение лекарств может проводиться разными способами:
- Перорально (внутрь). При таком способе введения в организм поступают таблетки, которые нужно проглатывать.
- Внутривенно (посредством инфузии). Препарат в виде готовой жидкости или раствора вводится внутривенно струйно или капельно.
- Внутрикатетерно (через тонкую гибкую трубку). На сегодняшний день это один из самых удобных и практичных методов. Трубка (катетер) помещается в крупную вену, часто в верхней части грудной клетки. Постоянно установленный катетер полезен для пациентов, которые нуждаются в различных лечебных процедурах. Вводя лечебные препараты непосредственно в катетер, а не в вену, можно избежать многих побочных эффектов, вызванных многократными инъекциями (дискомфорт, травмы и инфекции кожи, гематомы). Также данный метод позволяет вводить препараты микрокапельно, когда даже самые маленькие объемы препаратов вводятся в организм в течение длительного периода времени (часто более 24 часов). С этой целью используют специальное оборудование, называемое инфузоматом. Но особенно наличие катетера приветствуется в детской практике, поскольку позволяет свести болезненность лечения до минимума.
- Интратекально (в спинномозговую жидкость). Если при анализе спинномозговой жидкости, которая заполняет пространство вокруг спинного и головного мозга, обнаруживаются лейкозные клетки, врач может назначить интратекальную химиотерапию. Доктор вводит лекарства непосредственно в спинномозговую жидкость. Интратекальная химиотерапия может быть осуществлена двумя способами:
- пункцией – подача лекарства непосредственно в спинной мозг
- через катетер. Дети и некоторые взрослые пациенты получают химиотерапию с помощью специального катетера под названием резервуар Оммайа. Катетер устанавливается так, чтобы обеспечивать подачу препаратов в желудочки головного мозга. В него регулярно вводятся лекарства для лечения лейкоза. Этот метод позволяет избежать боли от пункций при необходимости введения лекарств в спинномозговую жидкость.
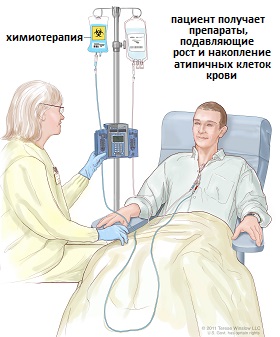
Рис.5 Химиотерапия (внутривенное введение)
Интратекальная терапия востребована, поскольку многие препараты, назначаемые внутривенно или перорально, не могут пройти через плотные стенки сосудов в головном и спинном мозге. Эта сеть кровеносных сосудов известна как гематоэнцефалический барьер.
Химиотерапия обычно дается в циклах. Каждый цикл имеет период лечения, за которым следует период отдыха. Введение препаратов возможно в стационаре, кабинете врача в поликлинике или даже в домашних условиях. Все зависит от индивидуальных особенностей каждого конкретного случая.
Побочные эффекты зависят, в основном, от того, какие сильнодействующие препараты даны и в каком количестве. Химиотерапия убивает быстро растущие клетки лейкемии, но препарат может также повредить и нормальные клетки, которые тоже обладают фазой быстрого роста. В основном это:
- Клетки крови. При химиотерапии падает уровень здоровых клеток крови. Этого достаточно, чтобы стать уязвимым для инфекций, часто получать синяки, обладать способностью к кровоточивости при малейших повреждениях, а также чувствовать себя очень слабым и усталым. Чтобы минимизировать риски, пациенты регулярно сдают анализы крови, чтобы проверить и скорректировать ее показатели. Если анализ неудовлетворительный, лечащий врач может остановить химиотерапию на время или уменьшить дозу препарата. Также есть лекарства, которые провоцируют активную выработку новых клеток крови. Или, возможно, потребуется переливание крови.
- Клетки корней волос. Химиотерапия может вызвать потерю волос. Если пациент потеряет волосы, впоследствии они отрастут, но могут несколько отличаться по цвету и фактуре.
- Клетки, которые выстилают желудочно-кишечный тракт. Химиотерапия может привести к ухудшению аппетита, тошноте и рвоте, диарее, а также язвам на губах и во рту. Пациент с подобными проблемами должен получать специальные лекарственные средства и другое лечение, которое поможет справиться с этими проблемами.
- Клетки половых систем (сперматозоиды или яйцеклетки). Некоторые виды химиотерапии могут привести к бесплодию.
В последнем случае прогноз во многом зависит от возраста пациента с лейкемией:
- Дети. Большинство детей, прошедших лечение лейкемии, впоследствии могут иметь детей. Однако все же, в зависимости от активности препаратов и полученных доз, возраста больного и особенностей его организма, некоторые мальчики и девочки могут быть бесплодными, как и взрослые.
- Взрослые мужчины. Химиотерапия может привести к повреждению клеток, занимающихся выработкой сперматозоидов. В ходе этого мужской организм может прекратить вырабатывать сперму с жизнеспособными половыми клетками. Подобные изменения в сперме могут быть постоянными, поэтому некоторые люди замораживает сперму до начала лечения и хранят ее в специализированном медицинском учреждении.
- Взрослые женщины. Химиотерапия может привести к повреждению яичников. Женщины могут иметь нерегулярные менструальные периоды или цикл может остановиться в целом. У некоторых наблюдаются все симптомы менопаузы, такие как приливы и сухость влагалища. Женщины, которые, возможно, захотят забеременеть в будущем, должны позаботиться о сохранении своих яйцеклеток перед началом лечения.
Несмотря на обилие побочных эффектов, данный вид терапии в большинстве случаев приносит желаемый результат и позволяет контролировать заболевание.
Целевая терапия при лейкозе
Люди с хронической миелоидной лейкемией, а некоторые - и с острым лимфобластным лейкозом, могут получать препараты, называемые «таргетной терапией». Таблетки «Иматиниб» (Гливек) были первым средством, одобренным для таргетной терапии хронического миелолейкоза. На сегодняшний день перечень препаратов для таргетной терапии расширился.
Целевые терапии основаны на эффективности препаратов, которые блокируют рост лейкозных клеток. Например, целевая терапия может блокировать действие аномального белка, который стимулирует рост клеток лейкемии. При этом нарушается процесс клеточного воспроизводства, и достигается хороший лечебный эффект.
Побочные эффекты подобного лечения включают припухлость, вздутие живота и внезапное увеличение веса. Целевая терапия также может привести к анемии, тошноте, рвоте, диареи, мышечным спазмам или кожной сыпи. Лечащий врач должен все время следить за проявлением признаков подобных проблем.
Биологическая терапия лейкоза
Некоторые люди с лейкемией в качестве лечения могут получить препараты из категории средств биологической терапии. Биологическая терапия при лейкозе представляет собой лечение, которое направлено на улучшение естественных защитных сил организма, позволяющих более активно противостоять болезни.
Одним из используемых в рамках биологического лечения препаратов является вещество, называемое моноклональным антителом. Метод введения его – капельный. Это вещество связывается с лейкозными клетками.
Залогом успешного внедрения моноклональных антител при лейкозе является наличие в их составе специального токсина, который убивает лейкозные клетки. Другой разновидностью воздействия является стимуляция иммунной системы и нацеливание ее на уничтожение лейкозных клеток.
В случае с хронической миелоидной лейкемией в качестве биологически активного вещества может быть использован препарат под названием интерферон. Он вводится под кожу или в мышцу. Его воздействие может замедлить размножение и рост лейкозных клеток. При таком заболевании другие биологические средства используются значительно реже, чем интерферон.
Стоит отметить, что пациентов не лечат по одной отработанной схеме. Каждый случай требует внимания и тщательной разработки терапевтической стратегии. Во время лечения терапия может быть скорректирована, дабы устранить имеющие место побочные эффекты.
Побочные эффекты биологической терапии отличаются от остальных. Чаще всего подобные вещества вызывают сыпь или отек в месте, где вводится препарат. Они также могут вызвать головную боль, мышечные боли, лихорадку или слабость. Лечащий врач может посоветовать сдать анализ крови, чтобы выявить признаки анемии и других проблем.
Лучевая терапия при лейкозе
Лучевая терапия (также называемая радиотерапией) использует лучи высокой энергии, чтобы убить лейкозные клетки. Люди получают лучевую терапию исключительно в больнице или клинике.
В одном случае облучению подвергаются участки тела, в которых собралось большего всего клеток лейкемии. Это может быть мозг, селезенка или любой другой орган. Этот тип терапии длится 5 дней из семи в течение нескольких недель.
В другом – проводится тотальное облучение, направленное на весь организм. Подобная методика предусматривает облучение один или несколько раз в день всего организма пациента. Ее часто используют, когда нужно быстро уничтожить клетки лейкемии перед проведением трансплантации стволовых клеток.
Побочные эффекты лучевой терапии зависят в основном от дозы радиации и частей тела, которые обрабатываются. Например, излучение на область живота может вызвать тошноту, рвоту и диарею. Кроме того, кожа в области, на которую направляют лучи, может стать красной, сухой и легко ранимой. Не исключена также потеря волос в области обработки.
Отметим, что переносится данная разновидность терапии лейкоза не очень хорошо. Особенно страдают пациенты, которые попадают к радиологу на сеанс лучевой терапии после нескольких недель предварительного лечения. Несмотря на то, что большинство больных чувствуют огромную усталость, все же врачи советуют пациентам стараться вести активный образ жизни.
Говоря о побочных эффектах лучевой терапии с пациентом, врачи всегда утверждают, что нечего бояться. Суть в том, что хотя они и вызывают опасения, но эти проявления также можно лечить или держать под контролем. Главное, чтобы пациент своевременно признался в том, что его состояние изменилось.
Стоит знать, что в большинстве своем побочные явления не являются стойкими и долговременными. Тем не менее, лучше обсудить с лечащим врачом возможные долгосрочные последствия лучевой терапии.
Трансплантация стволовых клеток при лейкозе
Некоторые люди с лейкемией в качестве перспективного метода лечения могут быть направлены на трансплантацию стволовых клеток. Предполагаемая пересадка стволовых клеток позволяет проводить массированный удар по болезни при помощи высоких доз лекарств и/или радиации.
Естественным результатом подобного активного лечения является полное уничтожение, как лейкозных, так и здоровых клеток в костном мозге. После чего пациент оказывается беззащитен перед любой инфекцией. После получения высокодозной химиотерапии, лучевой терапии или обоих методов в комплексе, пациенту для пополнения собственных запасов вводят внутривенно здоровые стволовые клетки через крупные сосуды.
По своей сути, данная методика похожа на переливание крови. Новые кровяные тельца в организме развиваются от пересаженных стволовых клеток. Новые клетки крови заменяют те, которые были разрушены в результате массированного лечения.
Трансплантация стволовых клеток проводится в больнице. Стволовые клетки могут быть взяты от самого пациента или от донора. В зависимости от того, какой путь выбирается, различается процедура трансплантации.
Источник стволовых клеток – сам пациент. Речь идет о пересадке аутологичных стволовых клеток от самого пациента. С этой целью до начала высокоактивного лечения большими дозами химиопрепаратов или активным облучением у пациента берут некоторое количество стволовых клеток. Чтобы подготовить их к пересадке, из их массы при специальной обработке извлекаются случайно попавшие лейкозные клетки. После того, как взятый у пациента материал будет очищен, его подвергают замораживанию и хранят положенное время. После того, как пациент закончит курс химиотерапии или радиационного облучения, клетки размораживают и используют для пересадки.
Источник стволовых клеток – неродственный донор или близкий член семьи в пределах первого поколения. Структура деятельности в данном случае напоминает предыдущую технологию за исключением нескольких этапов. При этом материал для трансплантации может быть взят у родителей, братьев или сестер пациента при наличии такой возможности. В некоторых случаях, когда родственники не могут выступить в роли доноров, для пациента могут подобрать донора из числа добровольцев, не являющихся ему родственниками. Выяснить, кто может быть донором, позволяет специальное исследование, проводимое медиками. Врачи, прежде всего, используют анализ крови, чтобы выяснить, каковы шансы на то, что клетки донора приживутся в организме реципиента.
Источник стволовых клеток – близнец. Если у пациента есть брат или сестра-близнец, то для пересадки могут использоваться стволовые клетки данного донора.
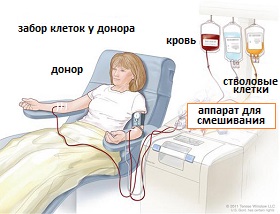
Рис.6 Подготовка клеток для трансплантация стволовых клеток
Источники забора стволовых клеток у доноров
Источник, из которого врачи получают стволовые клетки, не один. Первой методикой является изъятие клеток из крови (трансплантация периферических стволовых клеток). Второй – получение материала из костного мозга (трансплантация костного мозга). Третий метод – использование пуповинной крови для забора стволовых клеток. В последнем и менее распространенном случае пуповинную кровь при рождении человека собирают и хранят в замороженном виде, используя при необходимости для восстановления (трансплантация пуповинной крови).
Перенесенная процедура трансплантации не означает скорую выписку из стационара. После пересадки стволовых клеток больной остается в больнице в течение нескольких недель или месяцев. Это вызвано тем, что он подвергается риску инфекции и кровотечения из-за больших доз химиотерапии или облучения. После того, как пересаженные стволовые клетки начинают производить здоровые клетки крови, ситуация налаживается, и может быть принято решение о выписке.
Одной из проблем при проведении данной процедуры, точнее, ее осложнением, может стать некорректное поведение трансплантированных клеток. Подобная реакция может возникнуть у любого человека, который получает не собственные, а донорские стволовые клетки.
В силу тех или иных причин клетки, взятые у донора, могут принять за потенциальную угрозу, с которой стоит бороться, любые клетки организма реципиента. Чаще всего при этом поражаются клетки печени, кожи, желудочно-кишечного тракта. Подобная реакция может быть легкой или очень тяжелой. Причем процесс может начаться в любое время после трансплантации, даже годы спустя. В таком случае помочь могут стероиды и некоторые другие препараты.
Нужно ли другое мнение перед началом лечения?
Перед началом лечения большинство пациентов хочет услышать дополнительное мнение гематолога о диагнозе и плане лечения. Некоторые люди опасаются, что доктор обидится, если они попросятся проконсультироваться у кого-то иного. Но обычно все бывает наоборот.
Большинство врачей приветствуют подобный подход, и их ничуть не смущает подобное желание пациента. Данный пункт также внесен в страховку, поэтому если врач подпишет необходимое разрешение, страховка полностью покроет затраты на осмотр и диагностику в другой клинике.
Ожидать от посещения другого специалиста можно многого. Однако в большинстве случаев, или врач соглашается с диагнозом и планом терапии, намеченным первым специалистом, или может предложить другой подход. В любом случае, у пациента будет дополнительная информация и, возможно, большее чувство контроля. Подобное решение поможет чувствовать себя более уверенно, особенно зная, что диагноз поставлен точно, и ошибки нет.
Естественно, другое мнение нельзя получить за 5 минут. Это может занять некоторое время и усилия. Пациенту нужно собрать медицинские записи и записаться на прием к другому специалисту. В большинстве случаев понадобится не более пары недель, чтобы пройти диагностику и осмотр и получить результаты.
Задержка с началом лечения, как правило, не сделает лечение менее эффективным. Однако, чтобы уточнить, какова опасность откладывания лечения, нужно предварительно проконсультироваться у вашего основного лечащего врача. Ведь есть категория людей, которым терапия требуется очень срочно.
Есть много способов найти доктора для аналогичной консультации. Можно попросить лечащего врача, местное или государственное медицинское сообщество, обратиться в ближайшую больницу или медицинскую школу, чтобы уточнить ФИО специалистов. По телефону горячей линии для онкологических больных и в интернете можно почерпнуть недостающую информацию.
Нужна ли поддерживающая терапия при лейкозе?
Лейкемия и ее лечение могут привести к другим проблемам со здоровьем. Поэтому во время терапевтического процесса некоторым пациентам назначают поддерживающую терапию, которая будет проводиться до, во время или после лечения рака.
Поддерживающим будет являться то лечение, которое будет призвано предотвратить или помочь бороться с инфекциями, контролировать боль и другие симптомы. Также часто его назначают, чтобы уменьшить побочные эффекты терапии.
Помимо этого подобное лечение также поможет пациенту справиться с негативными чувствами, эмоциями и переживаниями, связанными с постановкой подобного диагноза. Таким образом, пациент может получить поддерживающую терапию, чтобы предотвратить или контролировать эти проблемы, улучшить комфорт и качество жизни во время лечения.
Инфекции. Люди, больные лейкемией, очень подвержены инфекциям, поэтому в качестве поддерживающей терапии им назначают антибиотики и другие препараты. Некоторые получают вакцины против гриппа и пневмонии. Помимо того врач может посоветовать пациенту избегать людных мест в период разгара простудных и других инфекционных заболеваний. Если же подобные меры не принесут результата, и пациент заболеет, то для него даже обычный насморк может иметь серьезные последствия. Поэтому к врачу за лечением нужно обращаться в кратчайшие сроки. Учитывая, что любая инфекция для незащищенного лейкоцитами организма может быть фатальной, вполне вероятно, что лечащий врач примет решение оставить инфицированного пациента в больнице для лечения.
Анемия и кровотечение. Анемия, кровотечения и другие проблемы с кроветворением часто требуют поддерживающей терапии. Скорее всего, больному регулярно будет требоваться переливание эритроцитов или тромбоцитов. Подобная мера сможет помочь в лечении анемии и снижении риска серьезного кровотечения.
Проблемы с зубами. Лейкемия и химиотерапия могут сделать рот чувствительным, легко инфицируемым, и повысят вероятность развития кровоточивости десен. В связи с этим врачи часто советуют пациентам регулярно обследоваться у стоматолога, а также пройти необходимый курс стоматологического лечения до начала химиотерапии. Стоматолог при этом должен подсказать пациенту, как сохранить свой рот чистым и здоровым на протяжении всего срока лечения.
Какое значение имеют питание и физическая активность при лейкемии?
Пациент, страдающий лейкозом, должен тщательно заботиться о себе, хорошо питаться и вести настолько активный образ жизни, насколько это возможно.
Ежедневно необходимо получать нужное количество калорий, чтобы поддерживать баланс и иметь оптимальный вес. Чтобы сохранить свои силы, следует в рационе иметь достаточно белка. Правильное питание может помочь больному чувствовать себя лучше и иметь больше энергии.
Иногда, особенно во время или вскоре после лечения, пациенту становится трудно кушать. Из-за дискомфорта или сильной усталости, вызванных самим заболеванием и активной терапией, аппетит пропадает и вовсе. Более того, меняется вкусовое восприятие. И те продукты, которые ранее нравились больному, теперь не кажутся ему настолько вкусными. Во многом на снижении аппетита сказываются побочные эффекты лечения (тошнота, рвота или язвы в полости рта). Врач, диетолог или другой медицинский работник должен предложить пути решения этих проблем.
Исследования показывают, что люди с раком чувствуют себя лучше, когда они активны. Прогулки, йога и другие виды деятельности могут помочь сохранить силу и увеличить энергию. Упражнения также могут уменьшить тошноту и боль, и сделать лечение легче.
Физическая активность также может помочь снять стресс. Правда, перед тем, как выбрать вид занятий, нужно поговорить с врачом. Кроме того, если во время занятий пациент будет испытывать боль, необходимо поставить в известность медперсонал.
Потребуется ли наблюдение по окончании курса терапии?
По окончании курса лечения больной будет нуждаться в регулярных осмотрах. Проверки помогут заметить любые изменения в состоянии здоровья, обнаружат начинающуюся инфекцию и помогут своевременно пройти симптоматическое лечение при наличии каких-либо осложнений. Если у пациента появились какие-либо проблемы со здоровьем, а пока на осмотр идти еще рано, следует обязательно обратиться к врачу.
Одной из важных целей регулярных осмотров является обнаружение возможного рецидива лейкемии. Даже тогда, когда рак, кажется, полностью побежден, болезнь иногда возвращается, потому что лейкозные клетки могли остаться где-то в теле и после лечения. Кроме того, осмотры помогают выявить проблемы со здоровьем, которые могут возникнуть в результате лечения рака.
Проверки могут включать в себя тщательный медицинский осмотр, анализы крови, цитогенетические анализы, рентгенографию, пункцию спинномозговой жидкости или взятие кусочка спинного мозга на анализ.
Почему важно организовать поддержку для больных лейкемией?
Диагноз лейкемии, поставленный больному, навсегда меняет жизнь его и его близких. Во многом с подобными переменами, которые затрагивают все сферы повседневного быта, бывает трудно справиться. Однако не стоит думать, что это что-то непреодолимое. С течением времени, когда больной примет свой диагноз и направит свои силы на лечение болезни, жизнь постепенно наладится и вернется в привычное русло.
Естественно, пока это не случится, жизнь любого больного человека будет полна различными опасениями. Основными из них становятся вопросы по поводу лечения, устранения или облегчения побочных эффектов, сроков пребывания в больнице, а также затрат на лечение. Однако, несмотря на это, очень важно не прекращать в этот момент заботиться о семье, постараться сохранить свою работу и продолжить вести повседневную деятельность.
Посильную поддержку пациентам с лейкозом должны оказывать:
- врачи, медсестры и другие медики, которые ответят на все насущные вопросы о работе, лечении, профилактике и т.д.;
- социальные работники, консультанты или религиозные деятели, с которыми можно поговорить о своих чувствах и переживаниях. Социальные работники могут обеспечить пациента дополнительной поддержкой и помощью, обеспечив, при необходимости, транспортировку, надомный уход, а также предложив элементарное человеческое сочувствие;
- группы поддержки, в которых помимо непосредственно больных принимают участие и те, кто уже излечился и на собственном примере может показать, что этот диагноз – не приговор. Помимо психологической поддержки для самих больных и членов их семей в подобных группах можно узнать о новых перспективных методах лечения, реакциях на ту или иную терапию.
Благодаря общению с другими людьми, человек на время забывает о проблемах, получает позитивные эмоции и настраивается на лучший исход. Также нередко именно через группы врачи находят добровольцев для тестирования новых методик лечения рака крови. А это имеет огромную важную роль.
Что собой представляют клинические испытания при лейкозе?
Все проведенные на сегодняшний день исследования рака привели к реальному прогрессу в лечении лейкемии. Из-за этих исследований взрослые и дети с лейкемией могут рассчитывать на улучшение качества жизни и получают меньше шансов умереть от этой болезни. Продолжая исследования, медики надеются, что в будущем можно будет успешно лечить данное заболевание в большинстве случаев.
Врачи по всему миру проводят много различных клинических испытаний (научные исследования, в которых люди участвуют добровольно). Клинические испытания предназначены, чтобы ответить на важные вопросы и выяснить, действительно ли безопасны и эффективны те или иные новые подходы.
Медики изучают методы новых и более эффективных способов лечения лейкемии, ищут способы улучшения качества жизни. Они испытывают новую целевую терапию, биологическую терапию и химиотерапию, а также работают с различными комбинациями лечения.
Даже если сами пациенты не получают личную выгоду от исследования, то они вносят важный вклад в науку, помогая врачам узнать больше о лейкемии и научиться контролировать данный патологический процесс. И хотя клинические испытания могут представлять определенный риск, врачи делают все возможное, чтобы защитить своих пациентов.

